На початку століття існували різні, часто суперечливі уявлення про те, як влаштований атом. Але більшість учених розділяли точку зору Дж. Дж. Томсона: атом — це рівномірно позитивно заряджена куля розміром близько 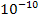 м, усередині якої "плавають" електрони, негативний заряд яких компенсує позитивний заряд, так що атом у цілому електрично нейтральний.
м, усередині якої "плавають" електрони, негативний заряд яких компенсує позитивний заряд, так що атом у цілому електрично нейтральний.
Хоч багато хто і згоджувався із такою моделлю атома, однак деякі фізики мали іншу точку зору. Так, ще в 1903 році японський фізик X. Нагаока стверджував інше: "...простори всередині атома величезні порівняно з розмірами електричних ядерець, які його утворюють, іншими словами, атом є своєрідною складною астрономічною системою, подібною до кільця Сатурна". Але така модель планетарного атома мала один нездоланний недолік. Електрон, що обертається по коловій орбіті, зазнає доцентрового прискорення, і відповідно до теорії Максвелла повинен випромінювати електромагнітні хвилі (зазаконами класичної електродинаміки не випромінює тільки заряд, що рухається прямолінійно з постійною швидкістю). Тому, втрачаючи енергію на випромінювання, електрон повинен упасти на позитивне ядро (це відбудеться дуже швидко — за час 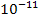 сек) і атом припинить існування. Іншими словами, така планетарна модель приводила до нестійкості атома. Однак, реальний атом стійкий, тому це не дозволяло ставитися з оптимізмом до такої планетарної моделі. Теорія Дж. Дж. Томсона не суперечила вимогам стійкості атома.
сек) і атом припинить існування. Іншими словами, така планетарна модель приводила до нестійкості атома. Однак, реальний атом стійкий, тому це не дозволяло ставитися з оптимізмом до такої планетарної моделі. Теорія Дж. Дж. Томсона не суперечила вимогам стійкості атома.
Вирішальну відповідь на питання про будову атома дав Ернест Резерфорд у результаті виконаних у 1909-1911 роках дослідів із розсіювання а-частинок (ядер гелію), які випромінює препарат радію, якщо на шляху цих а-частинок поставити металеву фольгу. Був проведений підрахунок кількості частинок, що розсіюються під різними кутами, а результати проведених за результатами експериментів розрахунків підтвердили, що атом має планетарну структуру. У 1911 році Резерфорд підбив підсумки проведених експериментів у своїй доповіді "Розсіювання а- і (3-променів і будова атома". Атом відповідно до висновків Резерфорда подібний до Сонячної системи: у центрі атома знаходиться позитивно заряджене ядро надзвичайно малих розмірів (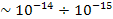 м), але в цьому ядрі зосереджена майже вся маса атома; навколо ядра на відстані -
м), але в цьому ядрі зосереджена майже вся маса атома; навколо ядра на відстані - 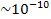 ом обертаються електрони. Це дуже нагадує Сонячну систему: планети теж обертаються навколо Сонця. Резерфорд спостерігав розсіювання а-частинок, спричинене атомами, — це результат відштовхування позитивно заряджених ядер гелію від позитивно заряджених ядер атомів.
ом обертаються електрони. Це дуже нагадує Сонячну систему: планети теж обертаються навколо Сонця. Резерфорд спостерігав розсіювання а-частинок, спричинене атомами, — це результат відштовхування позитивно заряджених ядер гелію від позитивно заряджених ядер атомів.
Експериментальне підтвердження гіпотези про планетарний атом не лише не вирішило, а, навпаки, загострило основне питання: адже електродинаміка стверджує, що така система існувати не може; електрон, що обертається за її законами, неминуче впаде на ядро. Потрібно було робити вибір: або електродинаміка, або планетарний атом. Щоб вийти із цього скрутного становища, потрібний був Нільс Бор.
При вирішенні цієї здавалося б нерозв'язної проблеми Бор вчинив так, як Олександр Македонський з Гордієвим вузлом: він не розплутував його, а розрубав мечем.
Значення робіт Резерфорда, які підтвердили справедливість планетарної моделі атома, дуже влучно охарактеризував Н. Бор: "Вирішальним моментом в атомній моделі Резерфорда було те, що вона з усією ясністю показала: стійкість атомів не можна пояснити на основі класичної фізики, і квантовий постулат — це єдино можливий вихід з гострої дилеми. Саме ця гострота невідповідності змусила мене абсолютно повірити в правильність квантового постулату".
Бор відразу ж став прихильником планетарної моделі. Утім, через багато років, у 1922 році, він скаже Гейзенбергу: "Я ніколи не сприймав планетарну систему буквально...".
Ключем до вирішення проблеми атомної стійкості були прості закони, що визначають спектр випромінювання елементів.
У1913 році Н. Бор сформулював свої знамениті постулати.
1-ий постулат — про стаціонарні стани. В атомі існують орбіти, рухаючись по яких електрон не випромінює.
2-ий постулат - про квантові стрибки. Електрон випромінює світло, тільки переходячи з однієї стаціонарної орбіти на іншу, тобто дискретними порціями. Коли електрон знаходиться на орбіті з щонайнижчою енергією, йому нікуди переходити (якщо він не одержує енергію ззовні). Так було пояснено стійкість атомів.
Бор переосмислив формулу Ейнштейна для фотоефекту, припустивши, .що частоту випромінюваного світла визначає співвідношення:
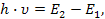
де 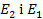 . — два можливих значення енергії атома.
. — два можливих значення енергії атома.
Але як визначити умову, що визначає стаціонарну орбіту? У будь-якого кругового руху, крім радіуса орбіти й швидкості руху по ній, є ще одна характеристика — момент кількості руху І, або орбітальний момент. Він дорівнює добутку маси на швидкість і на радіус орбіти, тобто:
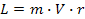
Бор стверджував: орбітальний момент електрона в атомі L не може бути довільним, він дорівнює цілому кратний від величини
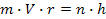
де n — ціле число: n - 1,2,3 ...
Ця умова дозволяє виділити стаціонарні орбіти (єдино можливі в атомі) з нескінченної кількості всіх, які тільки можна уявити. А оскільки в цьому виділенні основну роль відіграє квант дії h, то такий підхід називається квантуванням.
Стаціонарні орбіти (а, отже, і рівні енергії) нумеруються цілими числами п, що пробігають нескінченний ряд значень: n = 1, 2, 3 ... Ніякі інші рівні енергії, крім дозволених значень 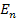 в атомі неможливі. Відсутність неперервності практично всіх характеристик руху електрона в атомі — його енергії, швидкості, радіуса орбіти — характерна риса квантової теорії.
в атомі неможливі. Відсутність неперервності практично всіх характеристик руху електрона в атомі — його енергії, швидкості, радіуса орбіти — характерна риса квантової теорії.
Потрібно відзначити, що успіх постулатів Бора визначався двома обставинами. По-перше, виконані відповідно до теорії Бора розрахунки лінійчастих спектрів елементів цілком збігалися з результатами спостережень; по-друге, розміри атомів (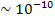 м), обчислені за формулою Бора, збігалися з передбаченнями кінетичної теорії матерії.
м), обчислені за формулою Бора, збігалися з передбаченнями кінетичної теорії матерії.
Незважаючи на незвичайність постулатів Бора, його теорія швидко набула визнання/тому що дозволяла групувати розрізнені раніше атомні явища навколо незрозумілої, але простої моделі.
Ці роботи Бора дали вирішальний поштовх усьому подальшому розвитку фізики, але тоді він ще не виявив себе як філософ, яким став пізніше. "Він виступив як фізик-теоретик із глибокою інтуїцією, схильний до оцінок і якісного розуміння явищ більшою мірою, ніж до їхнього математичного описування", — відзначає академік А. Б. Мігдал. Гейзенберг у статті "Квантова теорія і її інтерпретація" пише:
"Математична ясність сама по собі не мала для Бора якоїсь особливої цінності. Він побоювався, що формальна математична структура сховає фізичну сутність проблеми, і був переконаний, що закінчений фізичний опис повинен, безумовно, передувати математичному формулюванню".
Хоча теорія Бора й описувала всі найголовніші властивості атомів, зміст правил квантування залишався загадковим. Бор так і назвав ці правила постулатами, тобто недоведеними припущеннями.
Тільки геніальним осяянням можна пояснити те, що Бор осмислив свою теорію до того, як з'ясувалися хвильові властивості частинок.
Гейзенберг так писав про постулати Бора: "Мова образів Бора — це мова поезії, що лише почасти має стосунок до зображуваної ним дійсності і яку ніколи не можна розуміти буквально.... Постулати Бора подібні до пензля й фарб, які самі по собі ще не є картиною, але з їх допомогою можна її створити".
А в 1949 році Альберт Ейнштейн так згадував про епоху створення квантової механіки: "Усі мої спроби пристосувати теоретичні основи фізики до нових результатів зазнали невдачі. Це було так, неначе з-під ніг пішла земля й ніде не було видно твердого грунту, на якому можна було б будувати. Мені завжди здавалося чудом, що цієї хиткої основи, повної протиріч, виявилося досить, щоб дозволити Бору — людині з геніальною інтуїцією і тонким чуттям — встановити найголовніші закони спектральних ліній та електронних оболонок атомів, включаючи їх значення для хімії. Це мені здається дивом і тепер. Це — найвища музикальність в області думки".
У наш час ідеї Бора перетворилися з предмета науки на елемент культури — найвище, чого може досягти будь-як теорія.
З березня 1972 року космічна станція "Піонер-10" стартувала до Юпітера. На її борту знаходилася пластинка, на якій було вигравірувано інформацію, яку люди Землі вирішили повідомити іншим цивілізаціям: розміщення Землі в Сонячній системі, силуети чоловіка й жінки та схему атома водню.
У 30-і роки Нільс Бор відвідав Радянський Союз.Приїхавши до Грузії, в один із днів він із групою друзів відпочивав в Алазанській долині; неподалік від них розташувалися селяни, які пили вино Й співали пісні. Нільс Бор підійшов до них. "Це знаменитий фізик Нільс Бор", — почали пояснювати селянам грузинські фізики. Але тамада різким жестом зупинив їх пояснення, і, звертаючись до співтрапезників, проголосив тост: "Друзі! Наш гість — найбільший учений світу, професор з Данії Нільс Бор. Він створив атомну фізику. Його праці вивчають школярі всіх країн. Побажаємо йому і його супутникам довгих років життя, здоров'я і щастя!". Слова тамади тихо перекладали Бору, і коли тамада закінчив, із землі піднявся старий, підійшов до Бора, взяв обома руками руку Бора й поцілував її. Слідом піднявся інший горець, наповнив вином чашу і, вклонившись Бору, випив її. Бора вразила нереальність того, що відбувалося: він заплакав від подиву й подяки.
3.5.5 Співвідношення невизначеностей
3.5.6 Хвильова функція. Хвилі імовірності. Образ атома
3.5.7 Причинність класична і причинність квантова
3.5.8 Принцип додатковості
3.6 Світ елементарних частинок
3.6.1 Фундаментальні фізичні взаємодії
3.6.1.1 Гравітація
3.6.1.2 Електромагнетизм
3.6.1.3 Слабка взаємодія